Dãy chuyển động hóa học tập của kim loại gồm một dãy các kim loại mà dựa vào mức độ hoạt động vui chơi của nó tín đồ ta sẽ sắp xếp theo sản phẩm tự sút dần. Dãy vận động hóa học tập của sắt kẽm kim loại được hình thành thông qua việc triển khai nhiều thí nghiệm chất hóa học khác nhau. Dựa vào dãy vận động này, bọn họ sẽ dễ dàng dự đoán được khi một sắt kẽm kim loại phản ứng với những chất khác sẽ như thế nào. Dưới đây là phương pháp để các em học sinh lớp 9 hiểu rõ hơn về ý nghĩa sâu sắc và giải pháp học ở trong lòng dãy vận động hóa học tập của kim loại.
Bạn đang xem: Dãy hoạt dộng hóa học của phi kim
Các học thuộc lòng dãy vận động hóa học tập của kim loại lớp 9 dễ nhất

Nếu chỉ sử dụng kí hiệu hóa học sẽ khá khó nhằm ghi ghi nhớ dãy vận động hóa học tập của kim loại.
Tuy nhiên, bằng cách dưới đây các em học sinh sẽ dễ dãi học thuộc lòng hơn:
Khi (K) nào (Na) yêu cầu (Ca) thiết lập (Mg) Áo (Al) Záp (Zn) sắt (Fe) chú ý (Ni) sang trọng (Sn) buộc phải (Pb) Hỏi (H) Của (Cu) sản phẩm (Hg) Á (Ag) Phi (Pt) u (Au).
Giải thích:
Nhìn vào dãy vận động hoá học tập của sắt kẽm kim loại trên ta vẫn thấy nấc độ hoạt động hóa học của những kim loại giảm dần như sau:
K > mãng cầu > Ca > Mg > Al > Zn > fe > Ni > Sn > Pb > H > Cu > Hg > Ag > Pt > Au
Trong đó:
Các sắt kẽm kim loại mạnh chảy trong nước gồm có: K, Na, CaCác kim loại trung bình, KHÔNG tung trong nước bao gồm có: Mg, Al, Zn, Fe, Ni, Sn, PbCác kim loại yếu, không tan vào nước gồm có: Cu, Hg, Ag, Pt, Au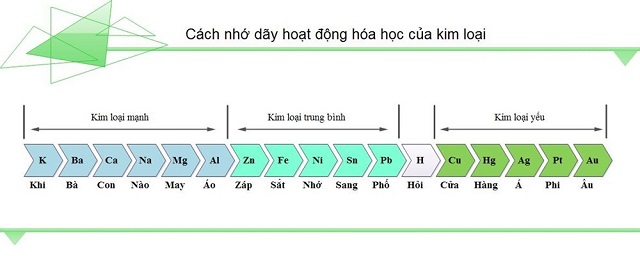
Dãy hoạt động hóa học của sắt kẽm kim loại lớp 9 có ý nghĩa sâu sắc gì?
Mức độ vận động hóa học của những kim loại sút dần từ bỏ trái thanh lịch phải.
Độ chuyển động hay còn được gọi là khả năng phản bội ứng của những kim loại bớt dần từ bỏ Li cho tới Au.
Xem thêm: Hướng Dẫn Sử Dụng Bao Cao Su Đúng Cách Dùng Bao Cao Su Nữ 18
Đặc trưng độc nhất là bội nghịch ứng cùng với nước. Khi 5 kim loại trước tiên đều tính năng dễ dàng cùng với nước ở điều kiện thường thì các kim các loại từ Mg trở đi nặng nề phản ứng (như sắt phải tác dụng ở ánh sáng cao) hoặc ko phản ứng như Au, Sn, Pb…v..v
Ví dụ:
Na, K sinh hoạt đầu hàng phản ứng mạnh khỏe với nước ở ánh sáng thường còn fe thì không.Fe tan trong axit HCl còn Cu, Ag không phản ứng được.Cu làm phản ứng được cùng với O2 còn Au thì không.Kim một số loại đứng trước Mg bội nghịch ứng cùng với nước ở đk thường giải tỏa khí H2
Ví dụ: 2Na + 2H2O ⟶ 2NaOH + H2

Kim nhiều loại đứng trước H phản nghịch ứng với một số axit (HCl, H2SO4 loãng,…) giải hòa khí H2
Ví dụ:
2K + 2HCl ⟶ 2KCl + H2Fe + 2HCl ⟶ FeCl2 + H22Al + 3H2SO4 ⟶ Al2(SO4)3 + 3H2Các kim loại Na, K chức năng với hỗn hợp thì đã phản ứng bên cạnh đó với nước cùng axit, nhưng có thể coi làm phản ứng cùng với axit trước với nước sau để xử lý bài tập.
Kim loại đứng trước (từ Mg trở đi) đẩy kim loại đứng sau ra khỏi dung dịch muối
Ví dụ:
Fe + CuSO4 ⟶ FeSO4 + CuCu + 2AgNO3 ⟶ Cu(NO3)2 + 2AgMg + FeCl2 ⟶ MgCl2 + FeChú ý:
Fe có muối hóa trị II với III nên có tương đối nhiều phản ứng sệt biệtVí dụ:
Fe + 3AgNO3 ⟶ Fe(NO3)3 + 3AgCu + 2FeCl3 ⟶ CuCl2 + 2FeCl2Fe + 2Fe(NO3)3 ⟶ 3Fe(NO3)2Cho Na, K vào hỗn hợp muối thì Na, K bội phản ứng cùng với nước trước tạo ra thành kiềm và kiềm sẽ tính năng tiếp với muối hạt (nếu tất cả phản ứng)Ví dụ: mang đến Na vào hỗn hợp muối CuSO4 thấy mở ra kết tủa với khí
2Na + 2H2O ⟶ 2NaOH + H2↑CuSO4 + 2NaOH ⟶ Cu(OH)2↓ + Na2SO4Kim loại chức năng với nước:
Một số kim loại hoạt động mạnh chức năng với nước để sinh sản bazơ khớp ứng và giải phóng hóa học khí là Hidro. Đây là đặc điểm khá rất gần gũi của những kim nhiều loại đứng đầu trong hàng – những kim loại mạnh nhất.
Phương trình hóa học:
Na+H2O→NaOH+H2↑Ba+2H2O→Ba(OH)2+H2↑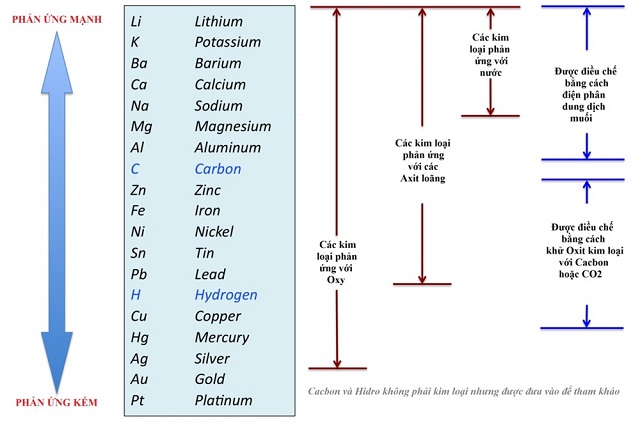
Kim loại tính năng với Axit tạo nên muối và giải phóng khí hidro
Các kim loại trong dãy phản ứng với axit tạo nên muối và khí hidro phải thỏa mãn hai điều kiện:
Kim một số loại đứng trước nhân tố hidro vào dãy vận động hóa họcDung dịch axit bội nghịch ứng bắt buộc là axit loãngVí dụ: Fe+2HCl——>FeCl2+H2
Kim loại chức năng với muối
Một ý nghĩa khá đặc biệt nữa được suy ra tự dãy vận động hóa học của kim loại đó là kim loại công dụng với muối. Bội nghịch ứng xẩy ra phải thỏa mãn nhu cầu các điều kiện sau:
Kim nhiều loại của đối kháng chất bắt buộc đứng trước sắt kẽm kim loại của hợp chất (xét trong địa chỉ của dãy chuyển động hóa học)Kim nhiều loại của solo chất phải bước đầu từ Mg trở về sau (tức là: Mg, Al, Zn…)Ví dụ: phản bội ứng giữa Mangan với muối bột của sắt: Mg+FeCl2—->MgCl2+Fe
Trên đấy là kiến thức về dãy hoạt động hóa học sắt kẽm kim loại và các tính chất cơ phiên bản của chúng. Hy vọng những tin tức trên để giúp đỡ các em nắm vững hơn kỹ năng và có thể áp dụng giải các bài toán có tương quan tới dãy hoạt động hóa học tập của kim loại lớp 9 này một cách xuất sắc nhất.












